Jupyter Notebook für die Analyse von Infinium MethylationEPIC v2.0 BeadChip-Daten in R
Die ChIP Analysis Methylation Pipeline (ChAMP)
Nachdem der Lab-Part der Methylierungsanalyse abgeschlossen ist, erhalten wir als Bioinformatiker*innen Datensätze zusammengesetzt aus einem Saplesheet und mehreren .idat Files, die Fluoreszenzsignale enthalten. Um diese Fluoreszenzsignale (binäres Dateiformat) auslesen und mit dem Samplesheet verknüpfen zu können, greifen wir auf bereits existierende Software zurück. In diesem Fall analysieren wir unsere Daten mit der ChIP Analysis Methylation Pipeline (ChAMP). Diese Pipeline basiert auf R und kombiniert bekannte Software für veschiedene Parts der Methylierungsnalyse (minfi, combat, bumphunter), um eine umfassende Pipeline zur Verfügung zu stellen.
ChAMP unterscheidet bei fast allen Funktionen zwischen drei Typen von Methylierungsarrays, da Illumina über die Jahre verschiedene Arrayversionen veröffentlicht hat. Die älteren Versionen sind 450k- und EPICv1-Arrays, die sich hauptsächlich in der Menge der enthaltenen CpGs unterscheiden. Dieses Notebook ist darauf ausgelegt, die Analyse von EPICv2-Arrays (die aktuellste Version) zu zeigen.
Die hier durchgeführten Schritte umfassen: 1) Einlesen und Filtern der Daten 2) Normalisierung der Methylierungslevel 3) Überprüfung auf und Entfernen von Batch-Effekten 4) Vergleich der Methylierung zwischen Zellproben
Eine Führung durch dieses Notebook als Video findet ihr hier:
- Part 1:
- Part 2:
Import aller nötigen R Pakete
# import all needed R packages
library(ChAMP)
library(ChAMPdata)
library(ggplot2)
library(stringr)
library(ggpubr)
Lade nötiges Paket: minfi
Lade nötiges Paket: BiocGenerics
Lade nötiges Paket: generics
Attache Paket: ‘generics’
Die folgenden Objekte sind maskiert von ‘package:base’:
as.difftime, as.factor, as.ordered, intersect, is.element, setdiff,
setequal, union
Attache Paket: ‘BiocGenerics’
Die folgenden Objekte sind maskiert von ‘package:stats’:
IQR, mad, sd, var, xtabs
Die folgenden Objekte sind maskiert von ‘package:base’:
anyDuplicated, aperm, append, as.data.frame, basename, cbind,
colnames, dirname, do.call, duplicated, eval, evalq, Filter, Find,
get, grep, grepl, is.unsorted, lapply, Map, mapply, match, mget,
order, paste, pmax, pmax.int, pmin, pmin.int, Position, rank,
rbind, Reduce, rownames, sapply, saveRDS, table, tapply, unique,
unsplit, which.max, which.min
Lade nötiges Paket: GenomicRanges
Lade nötiges Paket: stats4
Lade nötiges Paket: S4Vectors
Attache Paket: ‘S4Vectors’
Das folgende Objekt ist maskiert ‘package:utils’:
findMatches
Die folgenden Objekte sind maskiert von ‘package:base’:
expand.grid, I, unname
Lade nötiges Paket: IRanges
Lade nötiges Paket: GenomeInfoDb
Lade nötiges Paket: SummarizedExperiment
Lade nötiges Paket: MatrixGenerics
Lade nötiges Paket: matrixStats
Attache Paket: ‘MatrixGenerics’
Die folgenden Objekte sind maskiert von ‘package:matrixStats’:
colAlls, colAnyNAs, colAnys, colAvgsPerRowSet, colCollapse,
colCounts, colCummaxs, colCummins, colCumprods, colCumsums,
colDiffs, colIQRDiffs, colIQRs, colLogSumExps, colMadDiffs,
colMads, colMaxs, colMeans2, colMedians, colMins, colOrderStats,
colProds, colQuantiles, colRanges, colRanks, colSdDiffs, colSds,
colSums2, colTabulates, colVarDiffs, colVars, colWeightedMads,
colWeightedMeans, colWeightedMedians, colWeightedSds,
colWeightedVars, rowAlls, rowAnyNAs, rowAnys, rowAvgsPerColSet,
rowCollapse, rowCounts, rowCummaxs, rowCummins, rowCumprods,
rowCumsums, rowDiffs, rowIQRDiffs, rowIQRs, rowLogSumExps,
rowMadDiffs, rowMads, rowMaxs, rowMeans2, rowMedians, rowMins,
rowOrderStats, rowProds, rowQuantiles, rowRanges, rowRanks,
rowSdDiffs, rowSds, rowSums2, rowTabulates, rowVarDiffs, rowVars,
rowWeightedMads, rowWeightedMeans, rowWeightedMedians,
rowWeightedSds, rowWeightedVars
Lade nötiges Paket: Biobase
Welcome to Bioconductor
Vignettes contain introductory material; view with
'browseVignettes()'. To cite Bioconductor, see
'citation("Biobase")', and for packages 'citation("pkgname")'.
Attache Paket: ‘Biobase’
Das folgende Objekt ist maskiert ‘package:MatrixGenerics’:
rowMedians
Die folgenden Objekte sind maskiert von ‘package:matrixStats’:
anyMissing, rowMedians
Lade nötiges Paket: Biostrings
Lade nötiges Paket: XVector
Attache Paket: ‘Biostrings’
Das folgende Objekt ist maskiert ‘package:base’:
strsplit
Lade nötiges Paket: bumphunter
Lade nötiges Paket: foreach
Lade nötiges Paket: iterators
Lade nötiges Paket: parallel
Lade nötiges Paket: locfit
locfit 1.5-9.12 2025-03-05
Setting options('download.file.method.GEOquery'='auto')
Setting options('GEOquery.inmemory.gpl'=FALSE)
Lade nötiges Paket: ChAMPdata
Lade nötiges Paket: DMRcate
Lade nötiges Paket: Illumina450ProbeVariants.db
Lade nötiges Paket: IlluminaHumanMethylationEPICmanifest
Lade nötiges Paket: DT
Lade nötiges Paket: RPMM
Lade nötiges Paket: cluster
Keine Methoden in Paket 'RSQLite' gefunden für Anforderung: 'dbListFields' beim Laden von 'lumi'
Warning message:
"vorhergehender Import 'plyr::mutate' durch 'plotly::mutate' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plyr::rename' durch 'plotly::rename' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plyr::arrange' durch 'plotly::arrange' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plyr::summarise' durch 'plotly::summarise' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plotly::subplot' durch 'Hmisc::subplot' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plyr::summarize' durch 'Hmisc::summarize' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plyr::is.discrete' durch 'Hmisc::is.discrete' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'plotly::last_plot' durch 'ggplot2::last_plot' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'globaltest::model.matrix' durch 'stats::model.matrix' während des Ladens von 'ChAMP' ersetzt"
Warning message:
"vorhergehender Import 'globaltest::p.adjust' durch 'stats::p.adjust' während des Ladens von 'ChAMP' ersetzt"
>> Package version 2.29.1 loaded <<
___ _ _ __ __ ___
/ __| |_ /_\ | \/ | _ \
| (__| ' \ / _ \| |\/| | _/
\___|_||_/_/ \_\_| |_|_|
------------------------------
If you have any question or suggestion about ChAMP, please email to champ450k@gmail.com.
Thank you for citating ChAMP:
Yuan Tian, Tiffany J Morris, Amy P Webster, Zhen Yang, Stephan Beck, Andrew Feber, Andrew E Teschendorff; ChAMP: updated methylation analysis pipeline for Illumina BeadChips, Bioinformatics, btx513, https://doi.org/10.1093/bioinformatics/btx513 REQUIRE ChAMPdata >= 2.23.1
# set the location of the experiment directory
# the .idat fluorescence files and the samplesheet.csv have to be located inside the directory and it's subdirectories
epicv2_dir <- "../../example_datasets/epicv2/data"
Setzen des Datenverzeichnisses, Laden und Filtern der Daten
Alle Daten müssen für die Verarbeitung mit ChAMP in einem Verzeichnis abgelegt werden. Das Verzeichnis enthält sowohl alle .idat Dateien (jeweils grün und rot pro Probe), als auch das Samplesheet. ChAMP sucht initial eine .csv Datei, die als Samplesheet gelesen wird (bei mehr als einer .csv Dateien treten Probleme auf), liest daraus Sentrix_ID und Sentrix_Position, und sucht anhand dieser Informationen die .idat Dateien benannt in der Form Sentrix_ID_Sentrix_position_Grn.idat und Sentrix_ID_Sentrix_position_Red.idat.
Die Fluoreszenzsignale werden daraufhin ausgelesen und daraus je nach benötigtem Methylierungswert (methValue) Beta oder M Werte berechnet. Zusätzlich wird eine Reihe von Filtern angewendet, die folgende Sonden aus den Datensätzen entfernen: 1) Sonden, die nicht signifikant methyliert oder demethyliert sind (die sich nicht signifikant vom Hintergrundsignal unterscheiden) 2) Sonden, die nicht die Methylierung von CpGs überprüfen 3) Sonden, die in der Nähe von single nucleotide polymorphisms (SNPs) liegen 4) Sonden, die auf mehrere genomische Regionen mappen 5) Sonden, die auf dem X- und Y-Chromosom liegen 6) Sonden, in denen der Anteil der Proben mit weniger als 3 Beads über beadCutoff liegt
Zusätzlich werden Proben entfernt, in denen mindestens SampleCutoff Sonden durch vorherige Filterungsschritte entfernt wurden.
Alle fett gedruckten Begriffe sind Argumente der unten stehenden champ.load Funktion
Der Stdout und Stderr enthält von ChAMP sehr viele nützliche Informationen zu Datensatz und Filterprozess. So kann man beispielsweise sehen, wie viele Sonden in den verschiedenen Filterungsschritten entfernt wurden und, ob Proben entfernt wurden (abhängig von SampleCutoff).
# champ.load searches for a samplesheet file and all .idat files listed in samplesheet, extracts fluorescence values
myLoad <- champ.load(directory = epicv2_dir,
method="ChAMP", # replaces old loading method using minfi
methValue="B", # wether to calculate beta- or M-values
autoimpute=TRUE, # if values are missing uses the 3 most similar probes and uses the mean of their values for the missing value
filterDetP=TRUE, # filter single probes, whose methylation signal vs the background signal of the slide is not significant (detPcut)
ProbeCutoff=0, # remove all probes with higher missing-value-ratio
SampleCutoff=0.1, # remove a full sample if the failed probe ratio (based on p value) is higher than this threshold
detPcut=0.01, # significance p-value cutoff for filterDetP
filterBeads=TRUE, # filter out probes if the fraction of samples with a beadcount < 3 is higher than beadCutoff
beadCutoff=0.05, # acceptable fraction of samples with a beadcount < 3
filterNoCG=TRUE, # wether to remove non-cg probes
filterSNPs=TRUE, # wether to remove probes that fallnear a SNP (as defined in Nordlund et al. https://link.springer.com/article/10.1186/s13059-021-02529-2 )
population=NULL, # can be assigned to specific population according to www.internationalgenome.org/category/population/
filterMultiHit=TRUE, # wether to remove probes that align to multiple genomic locations (also according to Nordlund et al.)
filterXY=TRUE, # wether to remove probes on x and y chromosomes
force=FALSE, # minfi specific parameter
arraytype="EPICv2") # microarray type (can be one of "450K" "EPICv1" or "EPICv2")
[===========================]
[<<<< ChAMP.LOAD START >>>>>]
-----------------------------
[ Loading Data with ChAMP Method ]
----------------------------------
Note that ChAMP method will NOT return rgSet or mset, they object defined by minfi. Which means, if you use ChAMP method to load data, you can not use SWAN or FunctionNormliazation method in champ.norm() (you can use BMIQ or PBC still). But All other function should not be influenced.
[===========================]
[<<<< ChAMP.IMPORT START >>>>>]
-----------------------------
[ Section 1: Read PD Files Start ]
CSV Directory: ../../example_datasets/epicv2/data/Demo_EPIC-8v2-0_A1_SampleSheet_16.csv
Find CSV Success
Reading CSV File
Replace Sentrix_Position into Array
Replace Sentrix_ID into Slide
[ Section 1: Read PD file Done ]
[ Section 2: Read IDAT files Start ]
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R01C01_Grn.idat ---- (1/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R03C01_Grn.idat ---- (2/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R07C01_Grn.idat ---- (3/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R08C01_Grn.idat ---- (4/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R02C01_Grn.idat ---- (5/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R04C01_Grn.idat ---- (6/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R06C01_Grn.idat ---- (7/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R08C01_Grn.idat ---- (8/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R01C01_Grn.idat ---- (9/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R03C01_Grn.idat ---- (10/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R07C01_Grn.idat ---- (11/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R08C01_Grn.idat ---- (12/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R02C01_Grn.idat ---- (13/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R04C01_Grn.idat ---- (14/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R06C01_Grn.idat ---- (15/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R08C01_Grn.idat ---- (16/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R01C01_Red.idat ---- (1/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R03C01_Red.idat ---- (2/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R07C01_Red.idat ---- (3/16)
Loading:../../example_datasets/epicv2/data/206891110001/206891110001_R08C01_Red.idat ---- (4/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R02C01_Red.idat ---- (5/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R04C01_Red.idat ---- (6/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R06C01_Red.idat ---- (7/16)
Loading:../../example_datasets/epicv2/data/206891110002/206891110002_R08C01_Red.idat ---- (8/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R01C01_Red.idat ---- (9/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R03C01_Red.idat ---- (10/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R07C01_Red.idat ---- (11/16)
Loading:../../example_datasets/epicv2/data/206891110004/206891110004_R08C01_Red.idat ---- (12/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R02C01_Red.idat ---- (13/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R04C01_Red.idat ---- (14/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R06C01_Red.idat ---- (15/16)
Loading:../../example_datasets/epicv2/data/206891110005/206891110005_R08C01_Red.idat ---- (16/16)
Extract Mean value for Green and Red Channel Success
Your Red Green Channel contains 1105209 probes.
[ Section 2: Read IDAT Files Done ]
[ Section 3: Use Annotation Start ]
Reading EPICv2 Annotation >>
!!! Important, since version 2.29.1, ChAMP set default `EPIC` arraytype as EPIC version 2.
You can set 'EPIC' or 'EPICv2' to use version 2 EPIC annotation
If you want to use the old version (v1), please specify arraytype parameter as `EPICv1`.
For 450K array, still use `450K`
Fetching NEGATIVE ControlProbe.
Totally, there are 411 control probes in Annotation.
Your data set contains 411 control probes.
Generating Meth and UnMeth Matrix
Extracting Meth Matrix...
Totally there are 937055 Meth probes in EPICv2 Annotation.
Your data set contains 937055 Meth probes.
Extracting UnMeth Matrix...
Totally there are 937055 UnMeth probes in EPICv2 Annotation.
Your data set contains 937055 UnMeth probes.
Generating beta Matrix
Generating M Matrix
Generating intensity Matrix
Calculating Detect P value
Counting Beads
[ Section 3: Use Annotation Done ]
[<<<<< ChAMP.IMPORT END >>>>>>]
[===========================]
[You may want to process champ.filter() next.]
[===========================]
[<<<< ChAMP.FILTER START >>>>>]
-----------------------------
In New version ChAMP, champ.filter() function has been set to do filtering on the result of champ.import(). You can use champ.import() + champ.filter() to do Data Loading, or set "method" parameter in champ.load() as "ChAMP" to get the same effect.
This function is provided for user need to do filtering on some beta (or M) matrix, which contained most filtering system in champ.load except beadcount. User need to input beta matrix, pd file themselves. If you want to do filterintg on detP matrix and Bead Count, you also need to input a detected P matrix and Bead Count information.
Note that if you want to filter more data matrix, say beta, M, intensity... please make sure they have exactly the same rownames and colnames.
[ Section 1: Check Input Start ]
You have inputed beta,intensity for Analysis.
pd file provided, checking if it's in accord with Data Matrix...
pd file check success.
Parameter filterDetP is TRUE, checking if detP in accord with Data Matrix...
detP check success.
Parameter filterBeads is TRUE, checking if beadcount in accord with Data Matrix...
beadcount check success.
parameter autoimpute is TRUE. Checking if the conditions are fulfilled...
!!! ProbeCutoff is 0, which means you have no needs to do imputation. autoimpute has been reset FALSE.
Checking Finished :filterDetP,filterBeads,filterMultiHit,filterSNPs,filterNoCG,filterXY would be done on beta,intensity.
You also provided :detP,beadcount .
[ Section 1: Check Input Done ]
[ Section 2: Filtering Start >>
Filtering Detect P value Start
The fraction of failed positions per sample
You may need to delete samples with high proportion of failed probes:
Failed CpG Fraction.
HeLa 0.008623827
Jurkat 0.008777500
Raji 0.010284348
NA12873 0.007755148
NA12873_2_R 0.005907871
Raji_2_R 0.008498968
HeLa_2_R 0.009623768
Jurkat_2_R 0.013604324
HeLa_3_R 0.008403989
Jurkat_3_R 0.007717797
Raji_3_R 0.012234074
NA12873_3_R 0.009718746
NA12873_4_R 0.006075417
Raji_4_R 0.008782836
HeLa_4_R 0.010018622
Jurkat_4_R 0.014514623
Filtering probes with a detection p-value above 0.01.
Removing 30127 probes.
If a large number of probes have been removed, ChAMP suggests you to identify potentially bad samples
Filtering BeadCount Start
Filtering probes with a beadcount <3 in at least 5% of samples.
Removing 20547 probes
Filtering NoCG Start
Only Keep CpGs, removing 3445 probes from the analysis.
Filtering SNPs Start
!!! Important, since version 2.29.1, ChAMP set default `EPIC` arraytype as EPIC version 2.
You can set 'EPIC' or 'EPICv2' to use version 2 EPIC annotation
If you want to use the old version (v1), please specify arraytype parameter as `EPICv1`.
For 450K array, still use `450K`
Using general mask options
Removing 30398 probes from the analysis.
Filtering MultiHit Start
Filtering probes that align to multiple locations as identified in Nordlund et al
Removing 0 probes from the analysis.
Filtering XY Start
Filtering probes located on X,Y chromosome, removing 19986 probes from the analysis.
Updating PD file
Fixing Outliers Start
Replacing all value smaller/equal to 0 with smallest positive value.
Replacing all value greater/equal to 1 with largest value below 1..
[ Section 2: Filtering Done ]
All filterings are Done, now you have 832552 probes and 16 samples.
[<<<<< ChAMP.FILTER END >>>>>>]
[===========================]
[You may want to process champ.QC() next.]
[<<<<< ChAMP.LOAD END >>>>>>]
[===========================]
[You may want to process champ.QC() next.]
Qualitätskontrolle des Datensatzes vor der Normalisierung
Das Objekt MyLoad enthält, je nach methValue Beta- oder M-Werte für alle Sonden und Proben, die nach der Filterung übrig sind. Nach dem Filterungsprozess sollten die Daten visualisiert werden, um eine erste Qualitätskontrolle durchführen zu können.
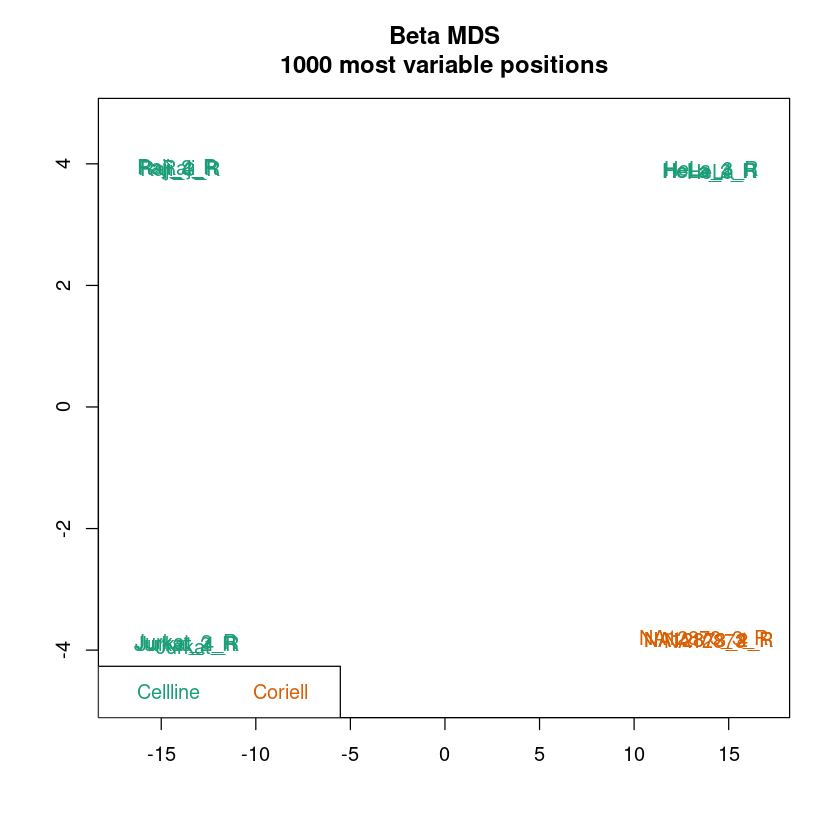
champ.QC erstellt uns aus dem Datensatz einen MDS-Plot, einen Density-Plot von Beta- oder M-Werten und ein Dendrogramm der Proben.
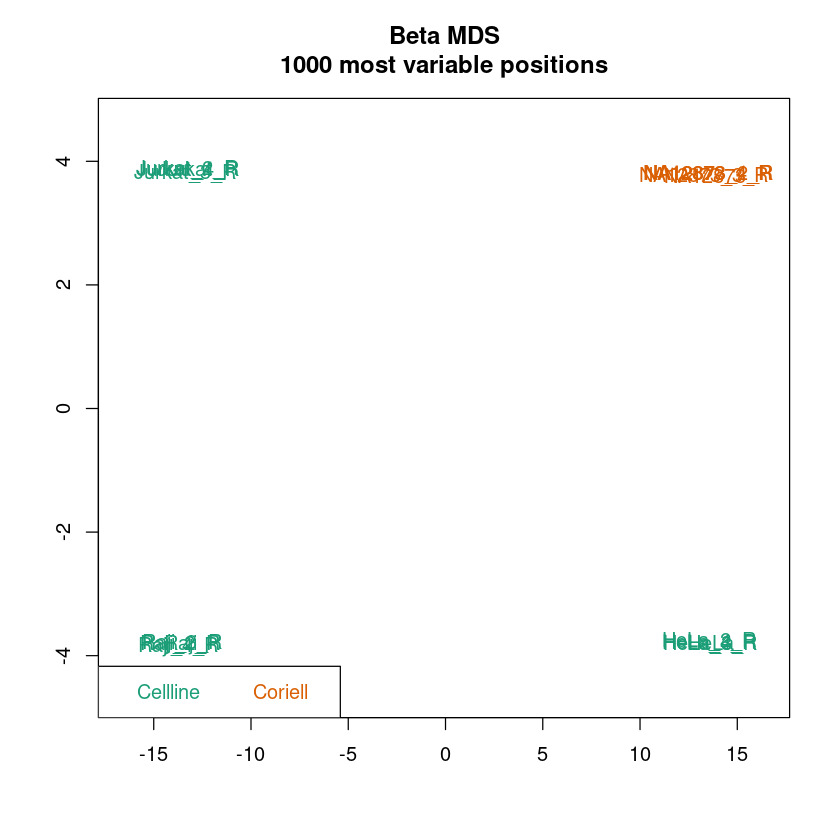
MDS-Plot: Ähnlich einer Principal component analysis (PCA) dient der MDS-Plot dazu, die Daten pro Probe in einen niedrigdimensionalen Raum zu projezieren. Für jede Probe bleiben zwei Werte übrig, die die Unterschiede zwischen den Proben bestmöglich beschreiben. Im Idealfall sollten Replikate sehr stark Clustern und die Samplegroups sollten in den meisten Fällen gut separiert sein.
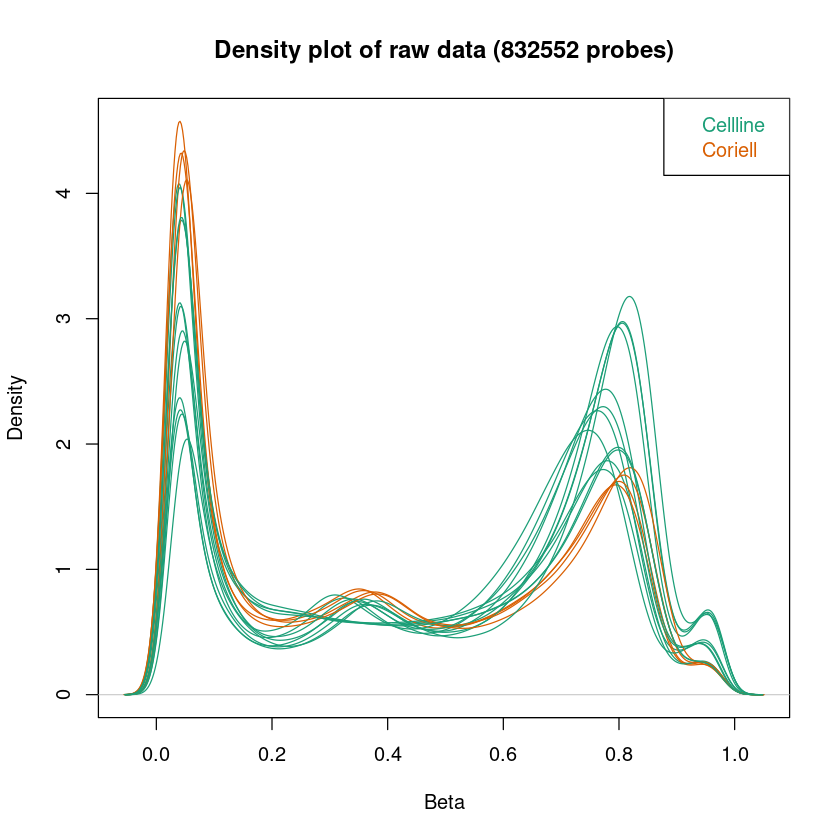
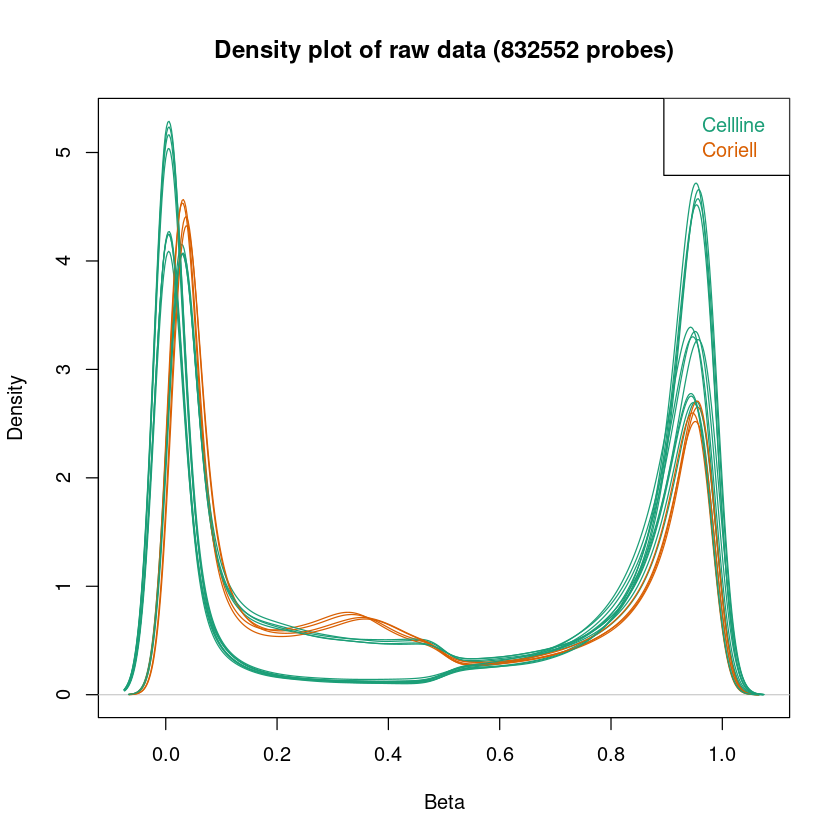
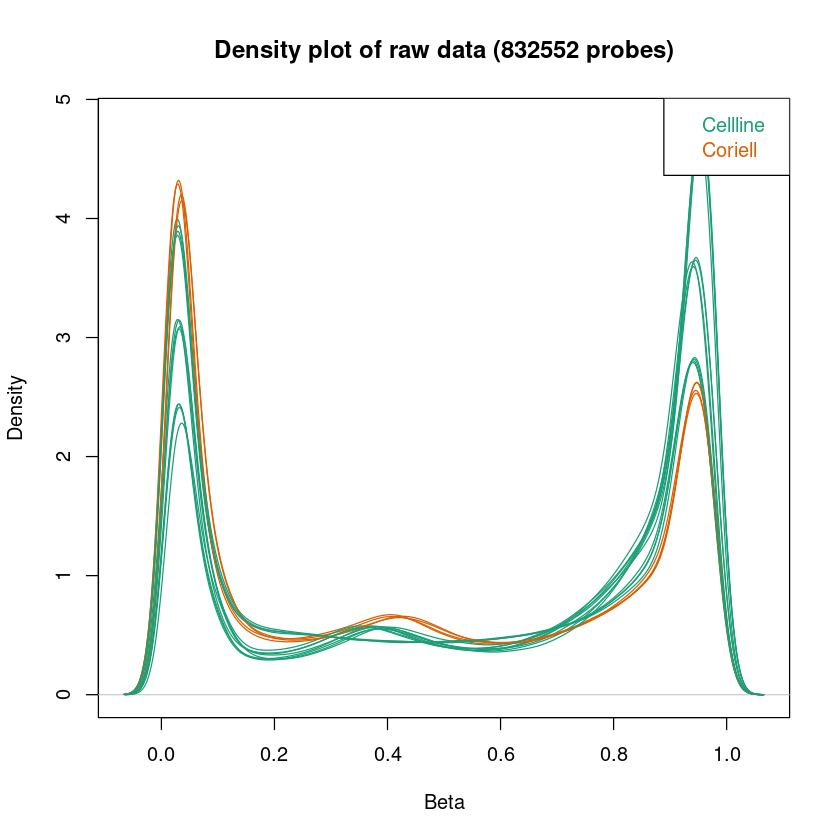
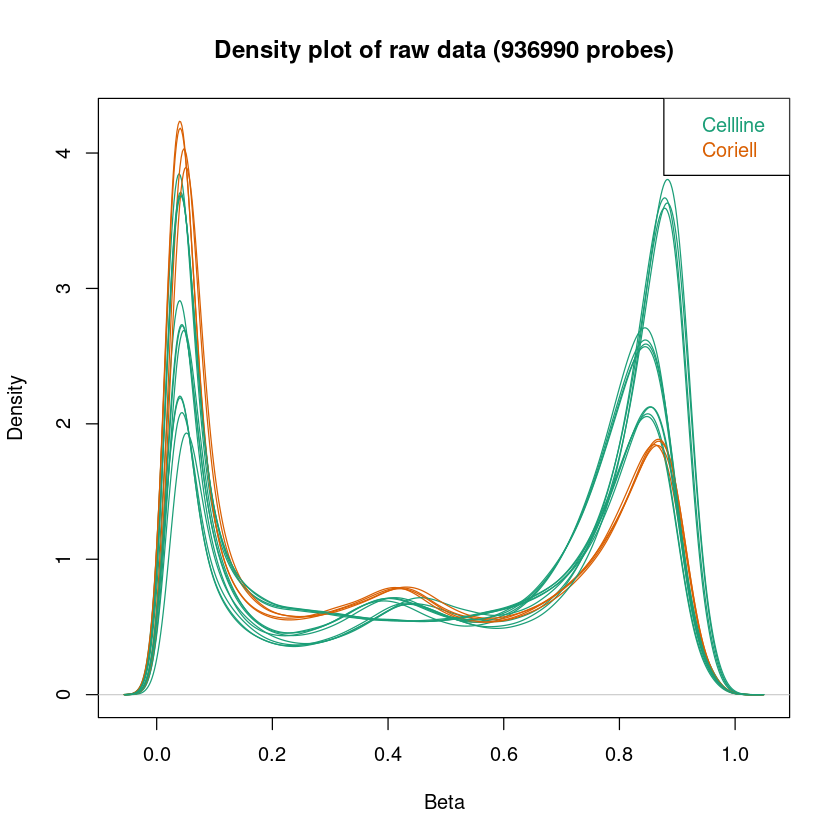
Density-Plot: Da die DNA, die wir auf die Microarrays geben aus einer Population von Zellen (keiner Einzelzelle) stammt, zeigt uns die Fluoreszenz die durchschnittliche Methylierung einer Menge von Zellen. Der Density-Plot zeigt die Dichteverteilung der Beta-Werte (Methylierung) pro Probe. Die hier dargestellten Kurven sollten eine Badewannen-Form haben: Zwei klare Peaks, der eine um 0, der andere um 1. Zwischen den beiden Peaks sollte die Kurve relativ flach sein. Diese Form ist zu erwarten, da wir annehmen, dass die Methylierung der meisten CpGs in einer Probe über mehrere Zellen gleich sein sollte - entweder methyliert oder unmethyliert.
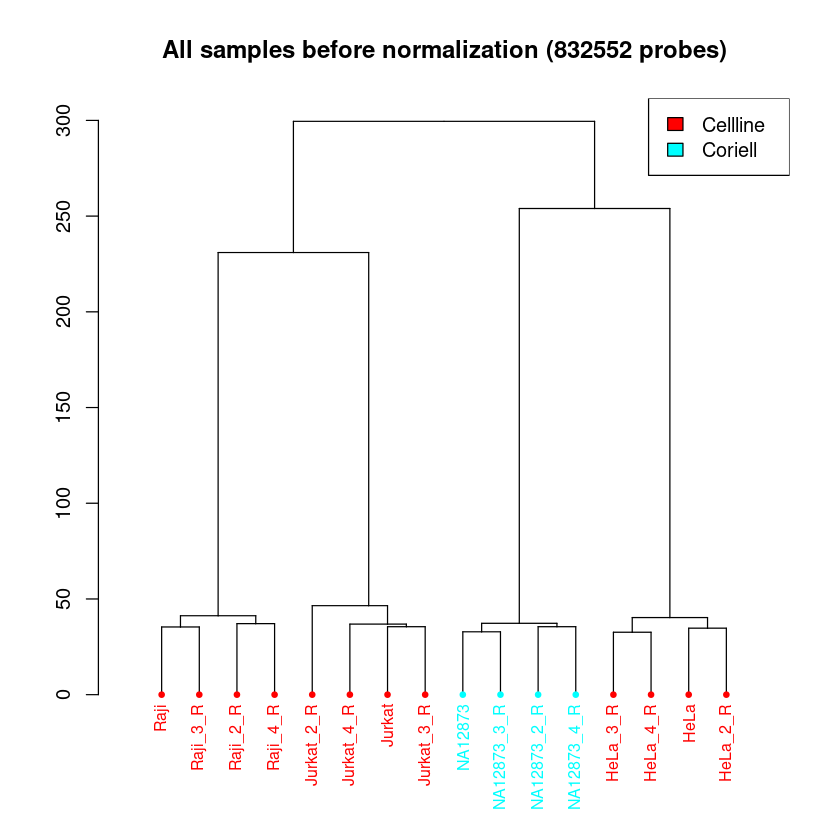
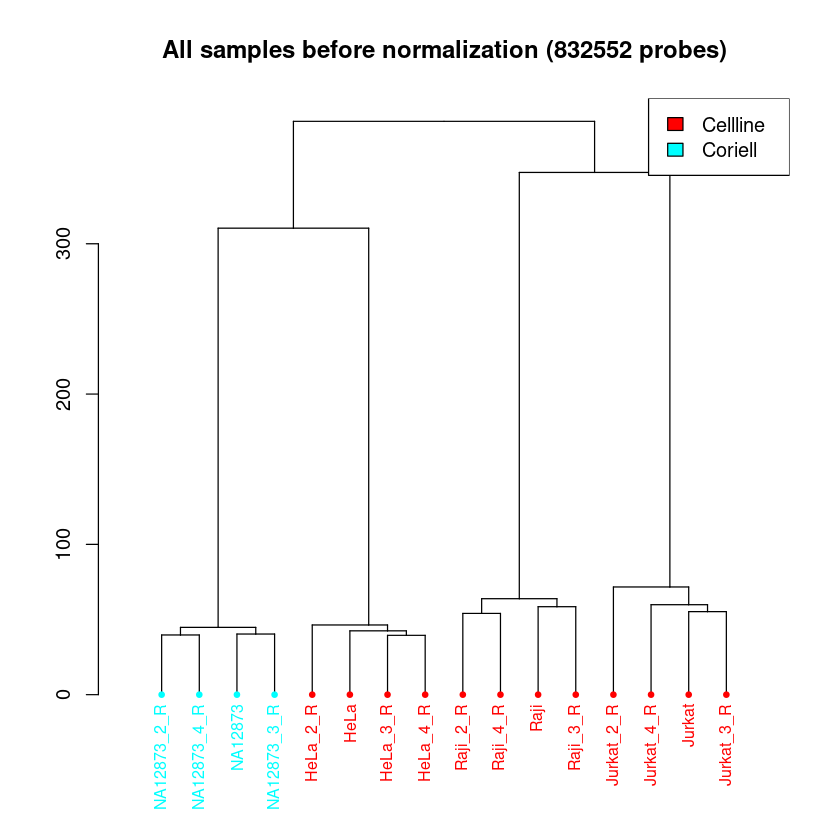
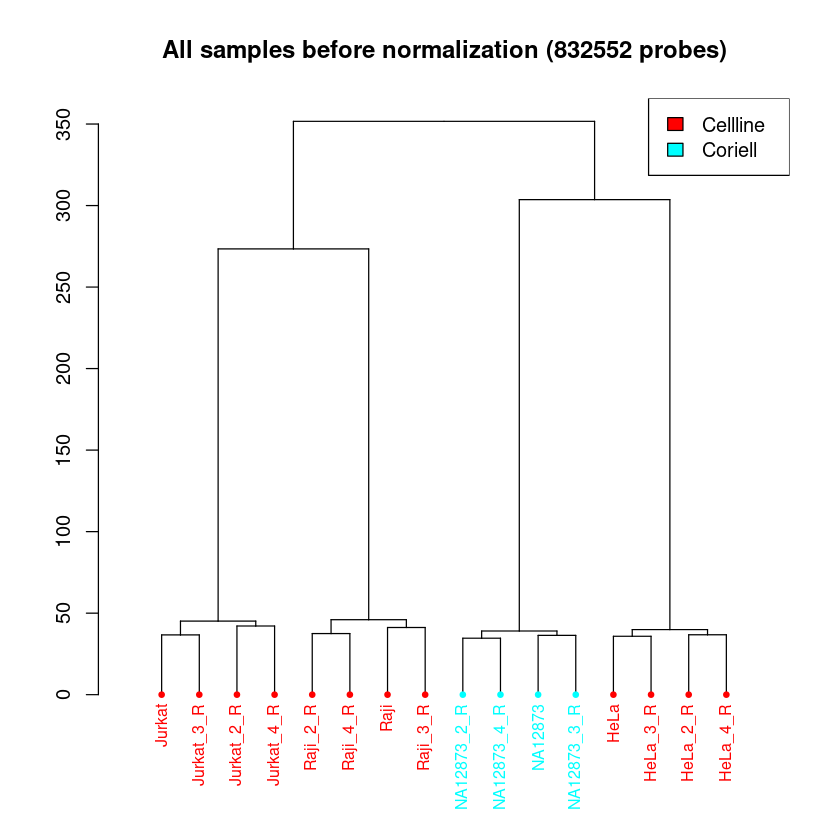
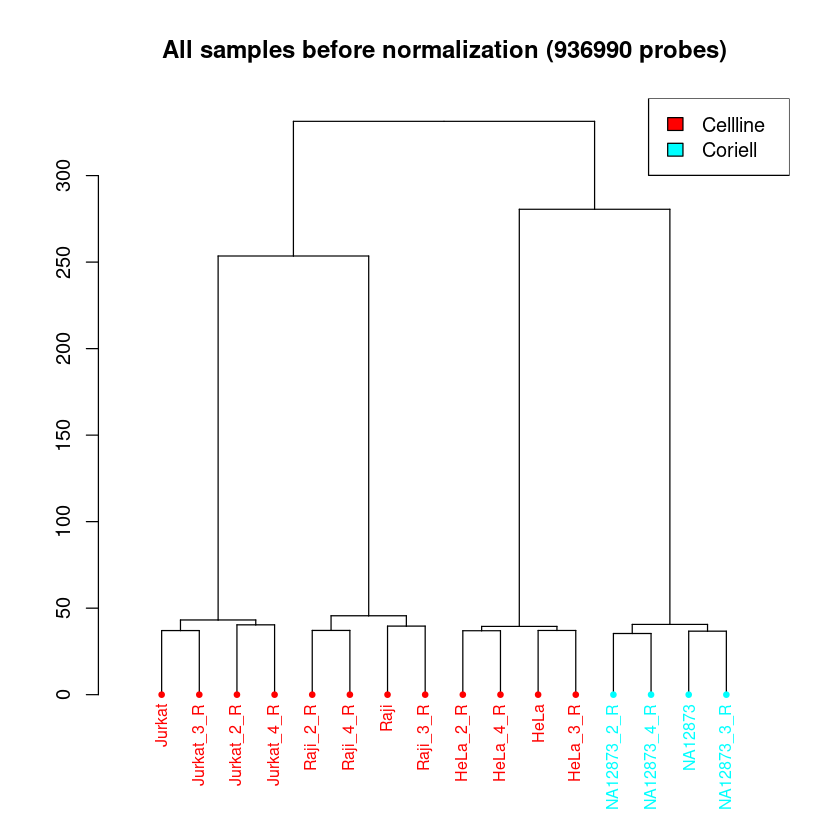
Dendrogramm: Das Dendrogramm hat eine ähnliche Funktion, wie der MDS-Plot. Hier werden alle Proben ihrer Ähnlichkeit entsprechend aufgetrennt. Die Länge des Weges zwischen zwei Proben spiegelt die Ähnlichkeit der Proben wieder. Hier ist zu erwarten, dass eine klare Separation der Proben zwischen den Samplegroups und Replikate stattfindet.
In allen Plots kann schon jetzt überprüft werden, ob die Samplegroups sich in Dendrogramm und MDS-Plot gut separieren. Das muss nicht immer der Fall sein, abhängig von den zu erwartenden Unterschieden in der Methylierung zwischen Samplegroups.
Wenn die Auftrennung der Proben in Samplegroups unerwartet schwach ist, kann dies darauf hindeuten, dass zwischen den Proben nur kleine Unterschiede in der Methylierung vorliegen. Wenn die Auftrennung der Replikate unerwartet groß sein sollte, kann dies darauf hindeuten, dass es im experimentellen Ablauf zu Batch-Effekten kam (mehr Info hierzu im Kapitel Erkennen und Entfernen von Batch Effekten). Um das genauer zu betrachten, könnt ihr pheno anpassen, um Auftrennungen nach anderen Spalten eures Samplesheets zu betrachten.
champ.QC(beta = myLoad$beta, # beta values stored in champ.load output
pheno=myLoad$pd$Sample_Group, # what samplesheet column is your phenotype (where do u expect the major difference between your samples)?
resultsDir="./CHAMP_QCimages/") # the plots will be saved in the directory this notebook file is located in
[===========================]
[<<<<< ChAMP.QC START >>>>>>]
-----------------------------
champ.QC Results will be saved in ./CHAMP_QCimages/
[QC plots will be proceed with 832552 probes and 16 samples.]
<< Prepare Data Over. >>
<< plot mdsPlot Done. >>
<< Plot densityPlot Done. >>
< Dendrogram Plot Feature Selection Method >: No Selection, directly use all CpGs to calculate distance matrix.
<< Plot dendrogram Done. >>
[<<<<<< ChAMP.QC END >>>>>>>]
[===========================]
[You may want to process champ.norm() next.]
Normalisierung mit anschließender Evaluation
Nachdem wir die Daten im oberen Abschnitt eingelesen und gefiltert haben, werden diese normalisiert, um die Vergleichbarkeit der Daten zu verbessern, ohne sie zu verfälschen. Dafür vergleichen wir den Effekt der Normalisierung durch PBC und BMIQ (unterschiedliche Normalisierungsmethoden). ChAMP bietet zusätzlich funktionale Normalisierung und SWAN, diese beruhen allerdings auf rgset und mset, weshalb wir sie an dieser Stelle nicht nutzen können.
Nach jeder Normalisierung nutzen wir erneut champ.QC, um eine Qualitätskontrolle durchzuführen. Am Ende entscheiden wir uns für die Normalisierung mit der besten Separation und der besten Badewanne (Density Plot).
# additional data needed for normalization
targets <- read.metharray.sheet(epicv2_dir)
rgset <- read.metharray.exp(targets = targets, recursive = TRUE)
mset <- preprocessRaw(rgset)
[read.metharray.sheet] Found the following CSV files:
[1] "../../example_datasets/epicv2/data/Demo_EPIC-8v2-0_A1_SampleSheet_16.csv"
Lade nötiges Paket: IlluminaHumanMethylationEPICv2manifest
Peak-based correction normalization (PBC)
# start with PBC normalization
myNormPBC <- champ.norm(beta = myLoad$beta, arraytype = "EPICv2", method = "PBC")
champ.QC(beta = myNormPBC, pheno = myLoad$pd$Sample_Group, resultsDir = "./CHAMP_QCimages/PBC/")
[===========================]
[>>>>> ChAMP.NORM START <<<<<<]
-----------------------------
champ.norm Results will be saved in ./CHAMP_Normalization/
[ SWAN method call for BOTH rgSet and mset input, FunctionalNormalization call for rgset only , while PBC and BMIQ only needs beta value. Please set parameter correctly. ]
<< Normalizing data with PBC Method >>
[1] "Done for sample 1"
[1] "Done for sample 2"
[1] "Done for sample 3"
[1] "Done for sample 4"
[1] "Done for sample 5"
[1] "Done for sample 6"
[1] "Done for sample 7"
[1] "Done for sample 8"
[1] "Done for sample 9"
[1] "Done for sample 10"
[1] "Done for sample 11"
[1] "Done for sample 12"
[1] "Done for sample 13"
[1] "Done for sample 14"
[1] "Done for sample 15"
[1] "Done for sample 16"
[>>>>> ChAMP.NORM END <<<<<<]
[===========================]
[You may want to process champ.SVD() next.]
[===========================]
[<<<<< ChAMP.QC START >>>>>>]
-----------------------------
champ.QC Results will be saved in ./CHAMP_QCimages/PBC/
[QC plots will be proceed with 832552 probes and 16 samples.]
<< Prepare Data Over. >>
<< plot mdsPlot Done. >>
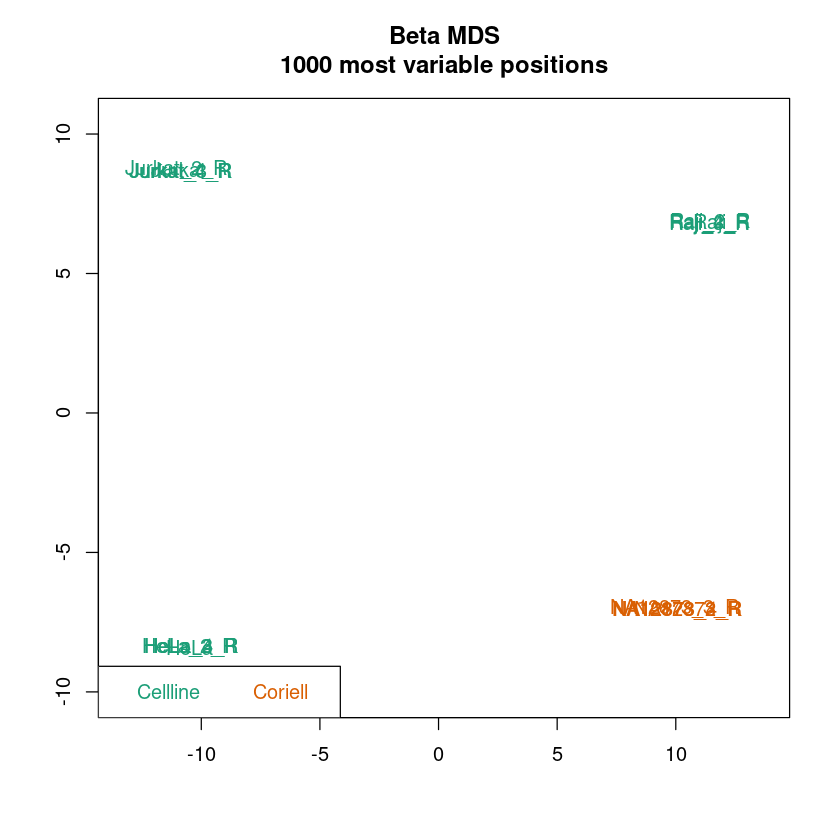
<< Plot densityPlot Done. >>
< Dendrogram Plot Feature Selection Method >: No Selection, directly use all CpGs to calculate distance matrix.
<< Plot dendrogram Done. >>
[<<<<<< ChAMP.QC END >>>>>>>]
[===========================]
[You may want to process champ.norm() next.]
Beta-mixture quantile normalization (BMIQ)
# BMIQ normalization
myNormBMIQ <- champ.norm(beta = myLoad$beta, arraytype = "EPICv2", method = "BMIQ")
champ.QC(beta = myNormBMIQ, pheno=myLoad$pd$Sample_Group, resultsDir="./CHAMP_QCimages/BMIQ/")
[===========================]
[>>>>> ChAMP.NORM START <<<<<<]
-----------------------------
champ.norm Results will be saved in ./CHAMP_Normalization/
[ SWAN method call for BOTH rgSet and mset input, FunctionalNormalization call for rgset only , while PBC and BMIQ only needs beta value. Please set parameter correctly. ]
<< Normalizing data with BMIQ Method >>
Note that,BMIQ function may fail for bad quality samples (Samples did not even show beta distribution).
3 cores will be used to do parallel BMIQ computing.
[>>>>> ChAMP.NORM END <<<<<<]
[===========================]
[You may want to process champ.SVD() next.]
[===========================]
[<<<<< ChAMP.QC START >>>>>>]
-----------------------------
champ.QC Results will be saved in ./CHAMP_QCimages/BMIQ/
[QC plots will be proceed with 832552 probes and 16 samples.]
<< Prepare Data Over. >>
<< plot mdsPlot Done. >>
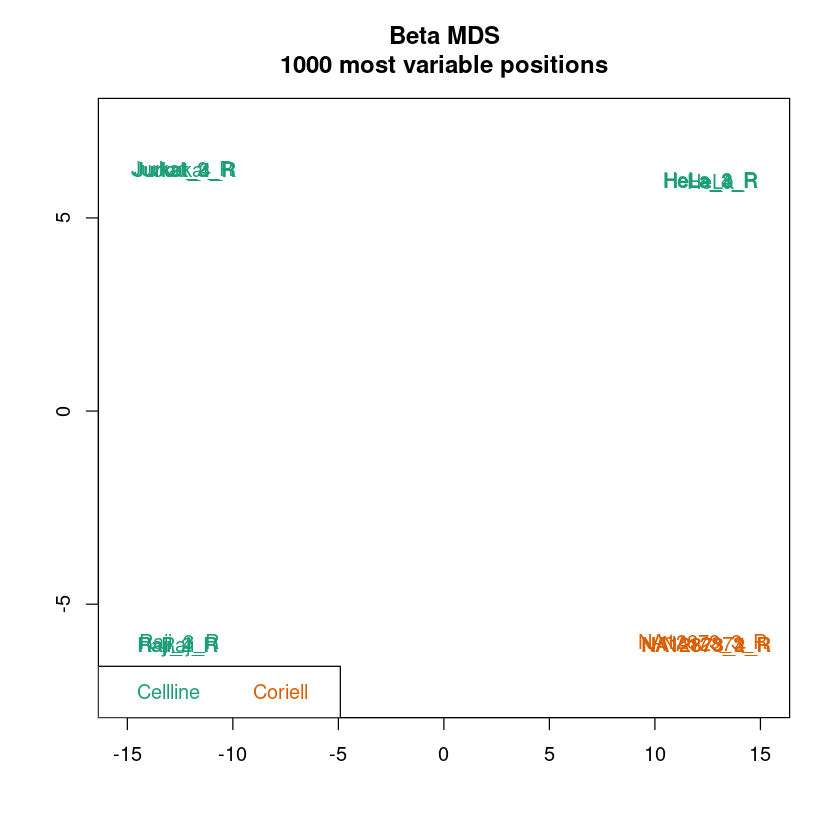
<< Plot densityPlot Done. >>
< Dendrogram Plot Feature Selection Method >: No Selection, directly use all CpGs to calculate distance matrix.
<< Plot dendrogram Done. >>
[<<<<<< ChAMP.QC END >>>>>>>]
[===========================]
[You may want to process champ.norm() next.]
Subset-quantiles within microarray normalization (SWAN)
# SWAN normalization (no native ChAMP support)
myNormSWAN <- champ.norm(arraytype = "EPICv2", method = "SWAN", rgSet=rgset,mset = mset,beta = NULL)
colnames(myNormSWAN) <- targets$Sample_Name
pheno <- targets$Sample_Group
names(pheno) <- targets$Sample_Name # Echte Namen
pheno <- pheno[colnames(myNormSWAN)] # Reihenfolge anpassen
champ.QC(beta = myNormSWAN, pheno = myLoad$pd$Sample_Group, resultsDir = "./CHAMP_QCimages/SWAN/")
[===========================]
[>>>>> ChAMP.NORM START <<<<<<]
-----------------------------
champ.norm Results will be saved in ./CHAMP_Normalization/
[ SWAN method call for BOTH rgSet and mset input, FunctionalNormalization call for rgset only , while PBC and BMIQ only needs beta value. Please set parameter correctly. ]
[>>>>> ChAMP.NORM END <<<<<<]
[===========================]
[You may want to process champ.SVD() next.]
[===========================]
[<<<<< ChAMP.QC START >>>>>>]
-----------------------------
champ.QC Results will be saved in ./CHAMP_QCimages/SWAN/
[QC plots will be proceed with 936990 probes and 16 samples.]
<< Prepare Data Over. >>
<< plot mdsPlot Done. >>
<< Plot densityPlot Done. >>
< Dendrogram Plot Feature Selection Method >: No Selection, directly use all CpGs to calculate distance matrix.
<< Plot dendrogram Done. >>
[<<<<<< ChAMP.QC END >>>>>>>]
[===========================]
[You may want to process champ.norm() next.]
# save best looking normalization result
myNorm <- myNormBMIQ
Erkennen und Entfernen von Batch Effekten
Es kann vorkommen, dass Daten selbst nach der Normalisierung noch nicht perfekt aussehen. “Nicht perfekt” bezieht sich hierbei auf erkennbare Unterschiede zwischen Proben, zwischen denen keine Unterschiede zu erwarten sind. Das können beispielsweise Replikate desselben Gewebes sein, die sich im MDS-Plot auftrennen.
In solchen Fällen kann die Ursache bei Batch-Effekten liegen. Als Batch-Effekt bezeichnet man (nicht zwingend erklärbare) Unterschiede in der durchschnittlichen Fluoreszenz zwischen verschiedenen Beadchips, Positionen auf dem Beadchip oder beispielsweise Tagen, an denen Experimente durchgeführt wurden.
Um diese Effekte zu finden, wird das Samplesheet und alle darin stehenden Gruppierungsspalten genutzt, um nach Unterschieden zwischen Gruppen zu suchen. Zu diesen Gruppen gehören Sample_Group, Sentrix_ID, Sentrix_Position und Pool_ID (falls ausgefüllt).
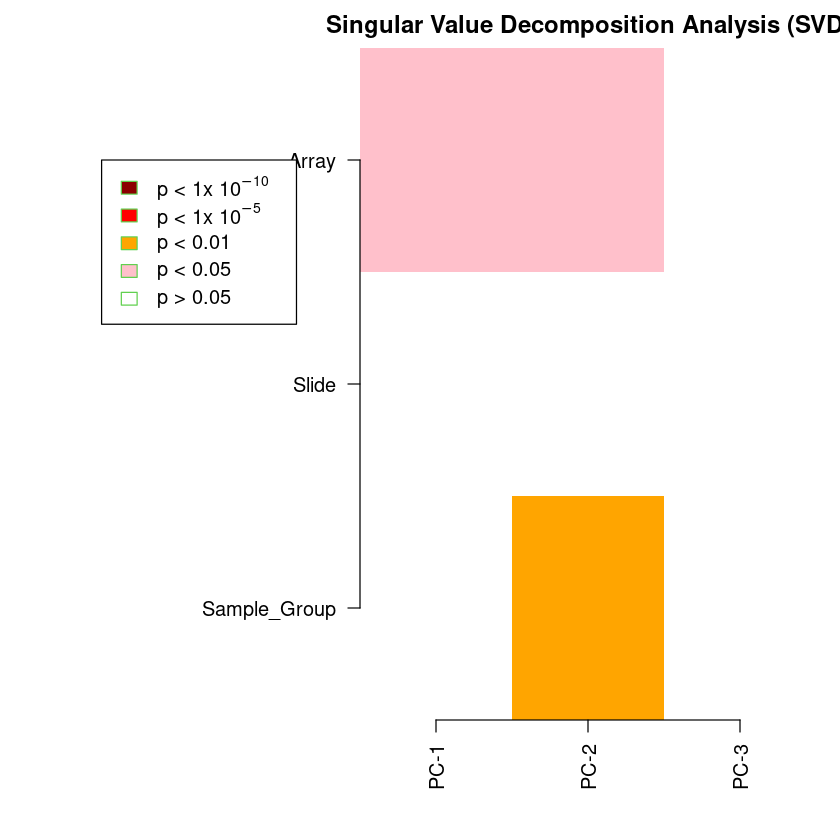
champ.SVD erstellt einen SVD Plot, in dem erkennbar ist, wie stark verschiedene Gruppierungsparameter mit Varianz zwischen den Proben (wiedergespiegelt durch die ersten drei Hauptkomponenten PC-1, PC-2 und PC-3) assoziiert sind. Alle bunten Blöcke sind dabei statistisch signifikant (p < 0.05) und sollten berücksichtigt werden mit Ausnahme der Blöcke für Samplegroup.
Nach Feststellung von Batch-Effekten kann champ.runCombat genutzt werden, um die gefundenen Batch-Effekte zu entfernen.
Zur Auswertung dient ein weiterer SVD-Plot.
champ.SVD(beta=myNorm,pd=myLoad$pd)
[===========================]
[<<<<< ChAMP.SVD START >>>>>]
-----------------------------
champ.SVD Results will be saved in ./CHAMP_SVDimages/ .
[SVD analysis will be proceed with 832552 probes and 16 samples.]
[ champ.SVD() will only check the dimensions between data and pd, instead if checking if Sample_Names are correctly matched (because some user may have no Sample_Names in their pd file),thus please make sure your pd file is in accord with your data sets (beta) and (rgSet).]
<< Following Factors in your pd(sample_sheet.csv) will be analysised: >>
<Sample_Group>(character):Cellline, Coriell
<Slide>(character):206891110001, 206891110002, 206891110004, 206891110005
<Array>(character):R01C01, R03C01, R07C01, R08C01, R02C01, R04C01, R06C01
[champ.SVD have automatically select ALL factors contain at least two different values from your pd(sample_sheet.csv), if you don't want to analysis some of them, please remove them manually from your pd variable then retry champ.SVD().]
<< Following Factors in your pd(sample_sheet.csv) will not be analysis: >>
<Sample_Name>
<Sample_Well>
<Sample_Plate>
<Pool_ID>
[Factors are ignored because they only indicate Name or Project, or they contain ONLY ONE value across all Samples.]
<< PhenoTypes.lv generated successfully. >>
<< Calculate SVD matrix successfully. >>
<< Plot SVD matrix successfully. >>
[<<<<<< ChAMP.SVD END >>>>>>]
[===========================]
[If the batch effect is not significant, you may want to process champ.DMP() or champ.DMR() or champ.BlockFinder() next, otherwise, you may want to run champ.runCombat() to eliminat batch effect, then rerun champ.SVD() to check corrected result.]
| Sample_Group | Slide | Array |
|---|---|---|
| 0.331975467 | 0.9624982 | 0.02799695 |
| 0.003609347 | 0.8974416 | 0.02607784 |
| 0.331975467 | 0.9541195 | 0.07487659 |
myCombat <- champ.runCombat(beta=myNorm,pd=myLoad$pd,batchname=c("Array"))
[===========================]
[<< CHAMP.RUNCOMBAT START >>]
-----------------------------
<< Preparing files for ComBat >>
[Combat correction will be proceed with 832552 probes and 16 samples.]
<< Following Factors in your pd(sample_sheet.csv) could be applied to Combat: >>
<Sample_Name>(character)
<Slide>(character)
<Array>(character)
[champ.runCombat have automatically select ALL factors contain at least two different values from your pd(sample_sheet.csv).]
<< Following Factors in your pd(sample_sheet.csv) can not be corrected: >>
<Sample_Well>
<Sample_Plate>
<Sample_Group>
<Pool_ID>
[Factors are ignored because they are conflict with variablename, or they contain ONLY ONE value across all Samples, or some phenotype contains less than 2 Samples.]
As your assigned in batchname parameter: Array will be corrected by Combat function.
<< Start Correcting Array >>
~Sample_Group
<environment: 0x61a34ce500f0>
Generate mod success. Started to run ComBat, which is quite slow...
Found 4 genes with uniform expression within a single batch (all zeros); these will not be adjusted for batch.
Found7batches
Adjusting for1covariate(s) or covariate level(s)
Standardizing Data across genes
Fitting L/S model and finding priors
Finding parametric adjustments
Adjusting the Data
champ.runCombat success. Corrected dataset will be returned.
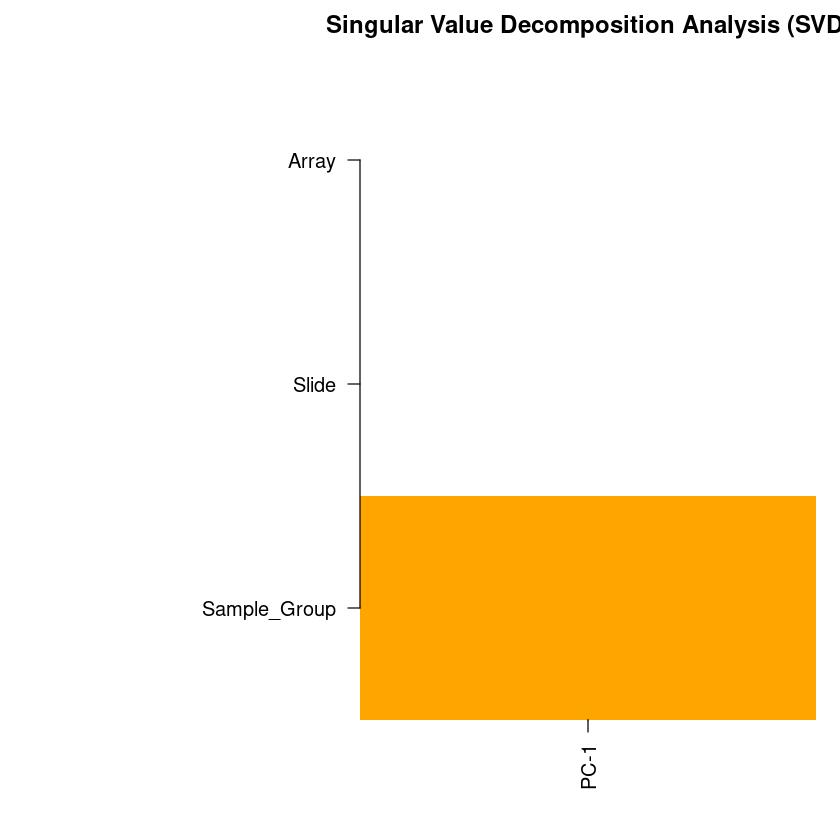
champ.SVD(beta=myCombat,pd=myLoad$pd)
[===========================]
[<<<<< ChAMP.SVD START >>>>>]
-----------------------------
champ.SVD Results will be saved in ./CHAMP_SVDimages/ .
[SVD analysis will be proceed with 832552 probes and 16 samples.]
[ champ.SVD() will only check the dimensions between data and pd, instead if checking if Sample_Names are correctly matched (because some user may have no Sample_Names in their pd file),thus please make sure your pd file is in accord with your data sets (beta) and (rgSet).]
<< Following Factors in your pd(sample_sheet.csv) will be analysised: >>
<Sample_Group>(character):Cellline, Coriell
<Slide>(character):206891110001, 206891110002, 206891110004, 206891110005
<Array>(character):R01C01, R03C01, R07C01, R08C01, R02C01, R04C01, R06C01
[champ.SVD have automatically select ALL factors contain at least two different values from your pd(sample_sheet.csv), if you don't want to analysis some of them, please remove them manually from your pd variable then retry champ.SVD().]
<< Following Factors in your pd(sample_sheet.csv) will not be analysis: >>
<Sample_Name>
<Sample_Well>
<Sample_Plate>
<Pool_ID>
[Factors are ignored because they only indicate Name or Project, or they contain ONLY ONE value across all Samples.]
<< PhenoTypes.lv generated successfully. >>
<< Calculate SVD matrix successfully. >>
<< Plot SVD matrix successfully. >>
[<<<<<< ChAMP.SVD END >>>>>>]
[===========================]
[If the batch effect is not significant, you may want to process champ.DMP() or champ.DMR() or champ.BlockFinder() next, otherwise, you may want to run champ.runCombat() to eliminat batch effect, then rerun champ.SVD() to check corrected result.]
| Sample_Group | Slide | Array |
|---|---|---|
| 0.003609347 | 0.9074465 | 0.4049149 |
Bestimmung und Visualisierung von differentiell methylierten Sonden (DMPs)
Nach erfolgreichem Laden der Daten, anschließendem Normalisieren und dem entfernen von Batch-Effekten kann jetzt final die Methylierung zwischen Gruppen von Interesse verglichen werden.
Dafür nutzen wir champ.DMP, was die Methylierung jeder Sonde zwischen zwei Gruppen (hier Samplegroups) vergleicht und testet, ob der Unterschied der Methylierung der Sonde zwischen den gruppen statistisch signifikant ist. Dabei kann jeweils nur ein Vergleich zwischen zwei Gruppen stattfinden. Gibt es mehr als zwei Samplegroups, werden alle paarweisen Vergleiche berechnet.
Die Visualisierung erfolgt hier nicht über Plots, die im Notebook sichtbar sind, sondern über eine interaktive HTML Darstellung, die über die angezeigte URL erreichbar ist.
Die daraufhin angezeigte Seite beinhaltet verschiedene Elemente:
- Eingabemaske (linker Rand): Hier müssen Nutzer einen P-Cutoff und einen FoldChange auswählen und auf Submit klicken, um DMPs anzeigen zu lassen. Über Gene Symbol kann man ein Gen auswählen, was daraufhin im Reiter Gene angezeigt wird. Über CpG ID Symbol kann man eine Sonde auswählen, die daraufhin im Reiter CpG einzeln angezeigt wird.
- DMPtable: Informationen zu den ausgewählten DMPs
- Heatmap: DMPs, die die SampleGroups am stärksten separieren
- Feature&Cgi: Positionen von DMPs in der DNA bzw. in CpG-Inseln
- Gene: Methylierung der DMPs eines Gens und Infos zu dem gewählten Gen
- CpG: Gene mit den meisten DMPs und einzelne CpGs
DMPs <- champ.DMP(beta = myCombat,pheno=myLoad$pd$Sample_Group, adjPVal = 0.05, arraytype = "EPICv2")
DMP.GUI(DMP=DMPs[[1]],beta=myCombat,pheno=myLoad$pd$Sample_Group)
[===========================]
[<<<<< ChAMP.DMP START >>>>>]
-----------------------------
!!! Important !!! New Modification has been made on champ.DMP():
(1): In this version champ.DMP() if your pheno parameter contains more than two groups of phenotypes, champ.DMP() would do pairewise differential methylated analysis between each pair of them. But you can also specify compare.group to only do comparasion between any two of them.
(2): champ.DMP() now support numeric as pheno, and will do linear regression on them. So covariates like age could be inputted in this function. You need to make sure your inputted "pheno" parameter is "numeric" type.
--------------------------------
[ Section 1: Check Input Pheno Start ]
You pheno is character type.
Your pheno information contains following groups. >>
<Cellline>:12 samples.
<Coriell>:4 samples.
[The power of statistics analysis on groups contain very few samples may not strong.]
pheno contains only 2 phenotypes
compare.group parameter is NULL, two pheno types will be added into Compare List.
Cellline_to_Coriell compare group : Cellline, Coriell
[ Section 1: Check Input Pheno Done ]
[ Section 2: Find Differential Methylated CpGs Start ]
-----------------------------
Start to Compare : Cellline, Coriell
Contrast Matrix
Contrasts
Levels pCoriell-pCellline
pCellline -1
pCoriell 1
You have found 685430 significant MVPs with a BH adjusted P-value below 0.05.
Calculate DMP for Cellline and Coriell done.
[ Section 2: Find Numeric Vector Related CpGs Done ]
[ Section 3: Match Annotation Start ]
[ Section 3: Match Annotation Done ]
[<<<<<< ChAMP.DMP END >>>>>>]
[===========================]
[You may want to process DMP.GUI() or champ.GSEA() next.]
Lade nötiges Paket: shiny
Attache Paket: 'shiny'
Die folgenden Objekte sind maskiert von 'package:DT':
dataTableOutput, renderDataTable
Listening on http://127.0.0.1:3016
Bestimmung und Visualisierung von differentiell methylierten Regionen (DMRs)
Nach der Evaluation von DMPs können diese zu DMRs zusammengefasst werden. Eine DMR ist eine Region, in der sich besonders viele DMPs befinden.
Die Visualisierung ist ähnlich der von DMPs in verschiedene Elemente aufgeteilt:
- Eingabemaske (linker Rand): Hier müssen Nutzer einen P-Cutoff und eine Mindestanzahl an enthaltenen DMPs angeben werden, um das Set der gefundenen DMRs vorzufiltern. Über den DMR-Index kann eine einzelne DMR anhand ihrer ID in DMRtable ausgewählt werden. Die gewählte DMR wird dann im DMRPlot visualisiert
- DMRtable: Zeigt die ausgewählten DMRs und viele Zusatzinformationen an
- CpGtable: Durchsuchbare DMP Tabelle in der die Zuordnung der DMPs zu den DMRs einsehbar ist. Sehr praktisch, um DMRs zu suchen, die ein bestimmtes Gen enthalten, da gene nur in CpGtable enthalten ist
- DMRPlot: Anzeige einer bestimmten DMR nach Selektion über die Eingabemaske
- Summary: Zeigt die Gene an, für die die meisten CpGs in einer oder mehrerer DMRs liegen, sowie der DMP-Status dieser CpGs. Zusätzlich sind die größten Methylierungsunterschiede zwischen CpGs in DMRs der Sample_Groups dargestellt
DMRs <- champ.DMR(beta=myCombat,pheno=myLoad$pd$Sample_Group,method="Bumphunter", arraytype="EPICv2")
DMR.GUI(DMR=DMRs, arraytype="EPICv2")
[===========================]
[<<<<< ChAMP.DMR START >>>>>]
-----------------------------
!!! important !!! We just upgrate champ.DMR() function, since now champ.DMP() could works on multiple phenotypes, but ProbeLasso can only works on one DMP result, so if your pheno parameter contains more than 2 phenotypes, and you want to use ProbeLasso function, you MUST specify compare.group=c("A","B"). Bumphunter and DMRcate should not be influenced.
[ Section 1: Check Input Pheno Start ]
You pheno is character type.
Your pheno information contains following groups. >>
<Cellline>:12 samples.
<Coriell>:4 samples.
[ Section 1: Check Input Pheno Done ]
[ Section 2: Run DMR Algorithm Start ]
<< Find DMR with Bumphunter Method >>
3 cores will be used to do parallel Bumphunter computing.
According to your data set, champ.DMR() detected 11309 clusters contains MORE THAN 7 probes within 300 maxGap. These clusters will be used to find DMR.
[bumphunterEngine] Parallelizing using 3 workers/cores (backend: doParallelMC, version: 1.0.17).
[bumphunterEngine] Computing coefficients.
[bumphunterEngine] Smoothing coefficients.
Lade nötiges Paket: rngtools
[bumphunterEngine] Performing 250 bootstraps.
[bumphunterEngine] Computing marginal bootstrap p-values.
[bumphunterEngine] Smoothing bootstrap coefficients.
[bumphunterEngine] cutoff: 0.184
[bumphunterEngine] Finding regions.
[bumphunterEngine] Found 16630 bumps.
[bumphunterEngine] Computing regions for each bootstrap.
[bumphunterEngine] Estimating p-values and FWER.
<< Calculate DMR success. >>
Bumphunter detected 13490 DMRs with P value <= 0.05.
[ Section 2: Run DMR Algorithm Done ]
[<<<<<< ChAMP.DMR END >>>>>>]
[===========================]
[You may want to process DMR.GUI() or champ.GSEA() next.]
!!! important !!! Since we just upgrated champ.DMP() function, which is now can support multiple phenotypes. Here in DMR.GUI() function, if you want to use "runDMP" parameter, and your pheno contains more than two groups of phenotypes, you MUST specify compare.group parameter as compare.group=c("A","B") to get DMP value between group A and group B.
[ Section 1: Calculate DMP Start ]
You pheno is character type.
Your pheno information contains following groups. >>
<Cellline>:12 samples.
<Coriell>:4 samples.
Your pheno contains EXACTLY two phenotypes, which is good, compare.group is not needed.
Calculating DMP
[===========================]
[<<<<< ChAMP.DMP START >>>>>]
-----------------------------
!!! Important !!! New Modification has been made on champ.DMP():
(1): In this version champ.DMP() if your pheno parameter contains more than two groups of phenotypes, champ.DMP() would do pairewise differential methylated analysis between each pair of them. But you can also specify compare.group to only do comparasion between any two of them.
(2): champ.DMP() now support numeric as pheno, and will do linear regression on them. So covariates like age could be inputted in this function. You need to make sure your inputted "pheno" parameter is "numeric" type.
--------------------------------
[ Section 1: Check Input Pheno Start ]
You pheno is character type.
Your pheno information contains following groups. >>
<Cellline>:12 samples.
<Coriell>:4 samples.
[The power of statistics analysis on groups contain very few samples may not strong.]
pheno contains only 2 phenotypes
compare.group parameter is NULL, two pheno types will be added into Compare List.
Cellline_to_Coriell compare group : Cellline, Coriell
[ Section 1: Check Input Pheno Done ]
[ Section 2: Find Differential Methylated CpGs Start ]
-----------------------------
Start to Compare : Cellline, Coriell
Contrast Matrix
Contrasts
Levels pCoriell-pCellline
pCellline -1
pCoriell 1
You have found 832552 significant MVPs with a BH adjusted P-value below 1.
Calculate DMP for Cellline and Coriell done.
[ Section 2: Find Numeric Vector Related CpGs Done ]
[ Section 3: Match Annotation Start ]
[ Section 3: Match Annotation Done ]
[<<<<<< ChAMP.DMP END >>>>>>]
[===========================]
[You may want to process DMP.GUI() or champ.GSEA() next.]
[ Section 1: Calculate DMP Done ]
[ Section 2: Mapping DMR to annotation Start ]
Generating Annotation File
Generating Annotation File Success
[ Section 2: Mapping DMR to annotation Done ]
Listening on http://127.0.0.1:3016